Технологии, секреты, рецепты
Содержание:
- Характеристики металла
- Оборудование для гальванопластики в домашних условиях
- Меднение металла с погружением в электролит.
- Методы нанесения (гальваническое, вакуумное, диффузионное, холодное и термическое напыление)
- Различные типы меднения
- Техника безопасности
- Зачем проводится меднение металлов
- Химическое осаждение металлов.
- Конверсионные процессы (Химическое оксидирование , Анодирование, химическое фосфатирование).
- Особенности гальванопластики
- Видео: Меднение в домашних условиях
- Раствор меднения для химической металлизации
- Состав растворов для химического меднения.
- Физиологическая роль меди.
- Технология меднения
Характеристики металла
Как уже было сказано выше, в природе медь, как правило, находится в виде небольших самородков.
Это уникальное вещество представляет собой достаточно тяжелый металл, который на вид напоминает самородок яркого розово-красного оттенка.
Этот металл обладает относительной мягкостью и высокой ковкостью, кроме этого, имеет температуру плавления порядка тысячи ста градусов по Цельсию.
Он великолепно проводит не только тепло, но и электрический ток, что и объясняет повышенный спрос на данный металл в электротехнике и приборостроении.
Всевозможные природные добавки в зависимости от различных факторов в металле могут варьироваться и различаться приблизительно от десяти до пятидесяти раз.
ВАЖНО ЗНАТЬ: Оборудование для литья алюминия в домашних условиях
Для данного металла большое значение имеет содержание в нем кислорода, и в зависимости от количества этого элемента в состав меди, разработана определенная классификация.
Так, медь может быть бескислородной и рафинированной.
Кроме этого, бывает медь с большим содержанием кислорода в своем составе, а также общего назначения, когда содержание кислорода максимальное.
Помимо данного элемента в этом металле также может находиться водород, попадающий туда за счет электролиза или отжига.
Медь имеет определенную кристаллическую решетку, и атомы водорода занимают в ней пространство в междоузлиях, а это значит, что на ее свойства они не оказывают практически никакого влияния.
Видео:
Если медь в своем составе содержит в определенном количестве кислород, то водород имеет свойство определенным образом взаимодействовать, но только при достаточно высоких температурах с медной закисью, и в этом конкретном случае начинает формироваться водяной пар, который имеет достаточно высокие показатели давления.
Это оказывает негативное влияние на металл в целом и может привести в некоторых случаях к образованию вздутий, а также трещинам и разрывам.
На изменении показателей пластичности у меди в худшую сторону могут оказать влияние присутствие железа, сурьмы.
Те примеси, которые относятся к группе малорастворимых, понижают хрупкость этого металла, но только при достаточно высоких внешних температурах, а это значит, что для меди крайне нежелателен процесс обработки горячим давлением.
На видео выше показано химическое меднение данного металла.
Оборудование для гальванопластики в домашних условиях
Гальваническое осаждение меди в домашних условиях проводят в емкостях любой геометрической формы. Размер гальванической емкости зависит от размера будущих изделий или репродуцируемых композиций. Материал может быть различным, подойдут емкости из стекла, керамики или пластмассы.
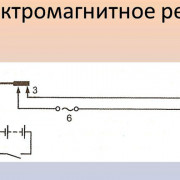
Вторым ключевым элементом гальванической установки является источник постоянного тока. Для проведения работ используют ток низкого напряжения в пределах 3-6 В. Можно использовать аккумулятор, или выпрямитель. Для измерения силы тока потребуется амперметр, для фиксации напряжения — вольтметр.
Для размещения формы и анодов в гальванической емкости необходимо предусмотреть подвесы. Форма подвешивается на проволоке из меди или латуни и помещается в емкость на расстоянии 15-20 мм от анода. Электроды, соединенные с положительной клеммой источника тока (анодом) подвешиваются также на меди или латуни, при этом проволочные крючки не погружают в электролит, в противном случае возможна деформация подвесов из-за разъедания крючка. Форма подключается к отрицательной клемме источника тока. В качестве анодов используют медные пластины толщиной от 3 мм. достаточных размеров. Площадь поверхности анодов должна превышать площадь поверхности формы.
Для контроля температуры электролита можно использовать обычный ртутный термометр.
Меднение металла с погружением в электролит.
Металлический предмет обработайте, как обычно,
наждачной бумагой, чтобы удалить оксидную пленку, протрите щеткой, как
следует промойте водой, обезжирьте в горячем содовом растворе и промойте
еще раз. В банку или стакан опустите на проволочках (лучше медных) две
медные пластинки — аноды. Между ними на проволочке же подвесьте деталь. Те проволочки, которые идут от медных
пластинок, соедините вместе и подключите к положительному полюсу источника
тока, а деталь — к отрицательному; включите в цепь реостат, чтобы регулировать ток, и миллиамперметр
(тестер). Источник постоянного тока с напряжением не более 6 В.
Раствор электролита для меднения: 20 г медного купороса и 2-3 мл серной кислоты на 100
мл воды — налейте в емкость, раствор должен полностью покрыть электроды.
Пользуясь реостатом, установите ток от 10 до 15
мА на каждый квадратный сантиметр поверхности детали. Минут через двадцать
выключите ток и выньте деталь — она покрыта тонким слоем меди. Чем дольше идет процесс, тем толще слой меди.
Методы нанесения (гальваническое, вакуумное, диффузионное, холодное и термическое напыление)
Существует несколько основных способов нанести хром на изделие:
Гальваническое хромирование. Заключается в осаждении металла на поверхность изделия под действием электрического тока. Если объяснять просто, изделие погружается в раствор с частичками хрома. На изделие подается электрический ток и частички начинают осаждаться на поверхности, тем самым образуя покрытие. На самом деле процесс очень сложный и дорогой. Метод актуален для металлических изделий (т.к. металл хорошо проводит ток).
Подробнее с гальваническим хромированием вы можете ознакомиться здесь
НПП Электрохимия выполняет полный цикл работ по нанесению гальванических хромовых покрытий. После нанесения покрытия и его проверки мы выдаем паспорт (сертификат) качества
Это особенно важно в рамках выполнения ГОЗ. Цена на хромирование оговаривается индивидуально с менеджером в зависимости от ТЗ
Вакуумное хромирование. Изделие погружается в вакуумную камеру с порошком. Порошок нагревается до температуры испарения и образует взвесь ионов в камере. Далее эта взвесь осаждается (бомбардировка ионами) на поверхности в виде конденсата, а затем кристаллизируется, образовывая покрытие.
Покрытие применятся в декоративных целях, особенно популярно для сувенирной и рекламной продукции (вывески, подарочная упаковка и т.д.). Отлично покрывается стекло и пластик. Идеально блестящей поверхности не всегда получается добиться, изредка покрытие осаждается неравномерно, видна шагрень (шишки). Не рекомендуется для изделий с требованиями по износостойкости.
Диффузионное хромирование. Процесс «насыщения»(заполнения) поверхности изделия хромом. Изделия погружают в порошок хрома и так же нагревают. Отличие от вакуумного метода состоит в том, что порошок не испаряется, а сразу «въедается» (диффундирует) в поверхность изделия. Примерно 50% покрытия находится внутри поверхности изделия, а 50% снаружи. Благодаря этому покрытие имеет превосходное сцепление с деталью.
Стандартный состав порошка: хром и каолин в соотношении 50 на 50. Плюс добавка (хлористый амоний/соляная кислота). Температура процесса — 1000° С, выдержка 6-15 часов.
Метод не из дешевых, но позволяет получить покрытие толщиной 100-300 мкм с хорошей адгезией и солидными защитными характеристиками.
Холодное распыление (мета-хромирование). Об этом методе мы поговорили в п.4. Просто распыление из баллончика или шланга. Красивая краска. Ни о каких защитных характеристиках и износостойкости речи быть не может. В интернете продается много готовых растворов для «хромирования» в различные цвета.
Термическое напыление. Методов достаточно много, но их объединяет одно – частицы металла нагревают до определенной температуры и с помощью направленного потока отправляют на изделие. Поток может быть газовый, пламенный, детонационный, электродуговой. Дешевый метод, применяется для изделий без высоких требований к защитным характеристикам покрытия. Подробнее можете прочесть здесь
Различные типы меднения
Меднение в домашних условиях могут выполнять даже новички в этом направлении. Чтобы получить качественное покрытие необходимо изучить все нюансы процедуры. Она может проводиться по одной из 2 технологий:
- Погружение в электролит. Заготовка погружается в жидкость и подается электроток. Обычно, используется в тех ситуациях, когда ее габариты не значительны.
- Без погружения в раствор. Более сложный процесс, но позволяющий достигать лучшего качества обмедненных поверхностей.
Во всех случаях необходимо подведение электричества, которое активизирует вещество.
Оптимальный метод выбирается в соответствии с поставленной целью:
- Формирование защитных и декоративных покрытий. Зачастую происходит смешение с никелем, хромом и медью. Получаются прочные и надежные поверхности.
- Защита при цементировании.
- Реставрация изделий.
Рассмотрим подробнее каждый из вариантов.
Омеднение с помещением в электролит
Наиболее доступный способ обмеднения в быту. Необходимы:
- Небольшого размера пластинки из меди.
- Проволока для проведения тока.
- Источник тока.
- Устройство для регулирования и измерения тока.
Последовательность действий:
- Чтобы растворить медь используется обыкновенный электролит, свободно продающийся или легко готовящийся своими руками. Для приготовления следует делать смесь серной кислоты с дистиллированной водой в пропорциях 3 к 100 миллилитрам. Нужная смесь получается после добавления в него 20 г медного купороса.
- Деталь следует очистить щеткой и наждачкой, чтобы удалить оксидную пленку.
- Провести обезжиривание раствором соды и промыть.
- Подготовленная емкость заполняется электролитическим раствором.
- В емкости размещаются 2 пластинки, подключенные к токопроводящей проволоке. Меж ними помещается деталь, которой предполагается омеднение. Нужно проверить полное закрытие смесью и пластинок, и заготовки.
- Затем пластины подключаются к плюсовому полюсу источника, а заготовка садится на минус. Предварительно желательно подключать амперметр и реостат. Выставить диапазон тока до 15 мА на 1см2 площади поверхности изделия.
- Выдержать в течение 20 минут.
- Выключается питание, заготовка извлекается из раствора. В итоге получается тонкое покрытие из меди. Продолжительность процесса оказывает влияние на толщину напыления. Благодаря технологии можно добиваться слоя до 300 мкм и более.
Метод возможно применять для обновления алюминиевых вещей, используемых в быту. Например, столовая утварь из алюминия после омеднения обретет вторую молодость.
Омеднение без помещения в раствор
Метод не предполагает залитие детали жидкостью. Он прекрасно подходит обработки цинковых или алюминиевых изделий.
Последовательность действий:
- Необходим провод – многожильный, медный. Снять изоляцию. Одна сторона распушается, делая подобие кисточки. Можно сделать что-то вроде рукояти для большего комфорта в работе. Другой край провода подключается к положительному полюсу источника тока. Напряжение – не больше 6 Вольт.
- Вышеописанным методом подготавливается электролит с медным купоросом. Посуда может использоваться любого типа, но лучше подобрать ту, которая позволит беспроблемно погружать кисточку из провода. Обрабатываемая деталь очищается от загрязнений. После этого проводами садится на отрицательный полюс источника тока.
- Процедура проводится следующим образом. Распушенный край-кисточка время от времени помещается в раствор. Ей следует проводить вдоль заготовки, не прикасаясь к ней. Поверхность нужно смочить электролитическим раствором. Во время обработки за счет отрицательного заряда деталь будет подтягивать ионы меди, покрываясь ими.
Это меднение металла подойдет для габаритных вещей, которые затруднительно поместить в емкость.
Техника безопасности
Иногда про технику безопасности при различных работах в домашних условиях рассказывают вскользь. Но при выполнении любых гальванических работ нужно строго соблюдать безопасность.
Опасность заключается в использовании токсичных химических веществ, высокой температуре нагрева раствора и повышенными рисками, которые сопровождают электрохимические реакции.
Лучше всего гальванические работы проводить в гараже или мастерской при обязательном проветривании или вентилировании помещения
Особое внимание следует уделить заземлению оборудования. Нужно соблюдать меры личной безопасности, а именно:
- Дыхательные пути следует защитить респиратором.
- Руки и запястья должны быть спрятаны в высокие и прочные резиновые перчатки.
- Обувь должна защищать от ожогов, а одежда прикрыта клеенчатым фартуком.
- Обязательно ношение специальных защитных очков.
Во время работы не рекомендуется ни пить, ни есть, чтобы в пищевод не попали вредные и опасные вещества.
Зачем проводится меднение металлов
Меднением называют нанесение на разные материалы и изделия тончайшего слоя меди. Обычно толщина этого слоя составляет 1-300 мкм. Именно медь обладает рядом свойств, которые делают ее пригодной для данной манипуляции. Она пластична, отлично поддается полировке. Гальванический пласт на стали после выполнения меднения почти не имеет пор.
Кроме того, медь характеризуется высокой электропроводностью и легко паяется. При использовании высокочастотных сигналов наибольшая плотность тока приходится на медный слой (скин-эффект), а общее сопротивление снижается.
Области применения технологии меднения обширны:
- создание промежуточного слоя перед хромированием и никелированием разных изделий (для снижения риска растрескивания при эксплуатации в сложных условиях);
- применение в гальванопластике;
- толстослойное покрытие сложных моделей и художественных образцов, производство копий разных изделий;
- изготовление радиотехнических, электротехнических деталей — контактов, проводников, антенн, волноводов;
- нанесение токопроводящего слоя на пластиковые изделия;
- защита металлопроката, листового железа, профилей.
Химическое осаждение металлов.
Процесс химического осаждения металлов (ХОМ) представляет собой окислительно-восстановительную реакцию. продуктом которой является металл:
Men+ + Red → Me + Ox
Термодинамическая вероятность такой реакции определяется разностью потенциалов восстановителя и окислителя, с одной стороны, и устойчивостью воды – с другой стороны, т. к. многие металлы разлагают воду и не могут быть выделены из водных растворов.
В качестве восстановителя могут быть использованы гипофосфит-ион, формальдегид, борогидрид, гидразин, ионы металлов переменной валентности (Sn2+, Ti3+ и др.). Соответствующие уравнения приведены в таблице 5. Термодинамически протекание какой-либо реакции возможно в той области рН и потенциалов, где устойчивы состояния продуктов этой реакции. Применительно к ХОМ это означает, что реакция протекает в области, где металл находится в восстановленной форме, а восстановитель — в окисленной. Для обеспечения протекания окислительно-восстановительного процесса ХОМ необходимо увеличение восстановительной способности восстановителя (например, формальдегида), что достигается смещением рН в сторону больших значений.Таблица 5 — Уравнения, описывающие системы “восстановитель-вода” в щелочных растворах.
|
№ |
Равновесие |
Уравнение, описывающее равновесие |
|
1 |
H2PO2-+H2O=H2PO3-+2H++2e |
E=-0,504-0,06pH |
|
2 |
HCHO+3OH-=HCOO-+2H2O+2e |
E=-0,19-0,09pH |
|
3 |
BH4-+OH-=BO2-+6H2O+8e |
E=-0,40-0,06pH |
|
4 |
N2H4+4OH-=N2+4H2O+4e |
E=-0,31-0,06pH |
|
5 |
HSnO2-+H2O+3OH-=Sn(OH)62-+6e |
E=-0,33-0,09pH |
|
6 |
Ti3+=Ti4++e |
E=-0,04 |
Конверсионные процессы (Химическое оксидирование , Анодирование, химическое фосфатирование).
Главное отличие этих процессов – Вы не наносите покрытие поверх изделия, а производите его из самого металла изделия. Грубо говоря, на поверхности образуется защитная корочка. Поэтому после покрытия размеры изделия практически не увеличиваются (защитная пленка растет вовнутрь)
Еще важное отличие – полярность. Для обычных покрытий изделие цепляют на «-», а аноды на «+»
Здесь же все наоборот. Изделие будет «+» и будет растворяться в процессе, а аноды должны быть на «-».
Химическое оксидирование (Хим.окс) применятся для стальных или алюминиевых изделий. После покрытия на поверхности образуется очень тонкая защитная корочка. (2-3мкм).
Анодирование (Ан.окс) – для алюминия. В этом случае защитная корочка толще (20-40мкм).
Фосфатирование (Хим.фос) – для стальных изделий. На поверхности образуется пленка из соли железа (фосфаты, 20-40мкм).

Рисунок 2 — Анодирование

Рисунок 3 — Химическое оксидирование

Рисунок 4 — Химическое фосфатирование
Покрытия отличаются относительно низкой стоимостью. (особенно Хим.окс)
Особенности гальванопластики
Гальванопластика — это электрохимический способ придания предмету определенной формы с помощью осаждения на него металла. Чаще всего этот метод используют при обработке металлом неметаллических предметов или при изготовлении копий ювелирных изделий.
Если при гальванопластике изделие не обладает электропроводящими свойствами, то его предварительно покрывают графитом, иногда бронзой. Затем мастер делает с копии слепок и начинает гальванический процесс. В качестве материала слепка используют гипс, графит или легко плавящийся металл.
Гальваника — это очень интересный и познавательный процесс, но он связан с активными веществами, которые могут навредить здоровью и нанести вред имуществу или окружающей среде. Поэтому перед тем как начинать гальванику своими руками, нужно принять все меры безопасности, изучить немного теории процесса и особенности поведения химических реактивов.
Видео: Меднение в домашних условиях
В этой инструкции я расскажу, как за несколько простых шагов покрыть медью металлическую шайбу. У вас будет обширное поле для экспериментов: вы можете поменять время, напряжение и состав кислот. Я пройдусь лишь по базовым шагам омеднения электролитическим способом, объясняя «как это сделать», но не вдаваясь в подробности «почему так происходит».
Кратко об эксперименте в домашних условиях: его цена варьируется в пределах 50-150 рублей, эксперимент займёт у вас 1 — 3 часа, а его сложность, в зависимости от ваших навыков гальванического меднения варьируется от лёгкой до средней.
Осторожно! Проводите эксперимент по меднению металла в хорошо вентилируемом помещении, а если вы молоды, то попросите взрослого помочь вам. Что вам понадобится:
Что вам понадобится:
- Медь — 2 небольших кусочка (в видео я использую медную проволоку, но в принципе подойдёт любой медный объект)
- Металлический объект, который мы будем покрывать медью (я взял шайбу)
- Стеклянный контейнер с крышкой
- Провода с зажимами-крокодилами x2
- Источник питания (предпочтительно с регулируемым напряжением)
- Уксус (который будет выступать в качестве кислоты)
- Инструмент для полировки (если хотите отполировать объект после омеднения)
Для этой инструкции я записал видео. В нём я прошелся по всем шагам омеднения, которые описаны ниже.
Раствор меднения для химической металлизации
В этой статье я расскажу вам как правильно приготовить раствор химического меднения, который является одним из этапов металлизации отверстий в печатных платах.
Приготовление раствора химической металлизации
Для приготовления раствора потребуются недорогие реактивы. Их можно купить в интернет магазинах, которых сейчас стало много и они работают с частными лицами. Трудностей с приобретением возникнуть не должно, было бы желание.
Порядок смешивания реактивов
1. Взвешиваем 30 гр. — медного купороса и 4 гр. — хлористого никеля. Наливаем в емкость 0,4 литра дистиллированной воды и растворяем эти реактивы в ней.
2. Взвешиваем 50 гр. — едкого натра, 20 гр. — кальцинированной соды и 85 гр. — трилона Б.
3. Наливаем в другую емкость 0,4 литра воды и растворяем реактивы в следующей последовательности.
Сначала едкий натр, затем кальцинированная сода и последним трилон Б.
4. Смешиваем эти растворы путем вливания раствора медного купороса с никелем, в раствор с трилоном Б, содой и едким натром. Хорошо перемешиваем и доводим объем раствора водой до 1 литра. Даем постоять 5..10 минут, если будет небольшой осадок, то фильтруем раствор.
5. Взвешиваем 1 гр. калия железосинеродистого (красная кровяная соль), растворяем его в 100 мл. дистиллированной воды. Затем берем шприцем 10 кубиков этого раствора — это будет 0,1 гр. этого реактива и добавляем его в только что приготовленный раствор раствора хим. меднения.
6. Взвешиваем 1 гр. калия роданистого и растворяем его в 100 мл. дистиллированный воды. Затем берем шприцем 0,3 кубика этого раствора — это будет 0,003 гр. и также добавляем его к основному раствору.
Калий железосинеродистый и калий раданистый являются ядовитыми веществами. При работе с ними соблюдайте элементарную технику безопасности. Не нюхайте, не пробуйте на вкус и т.п. При размешивании раствора, работайте в резиновых перчатках!!!
7. Хорошо перемешиваем раствор хим. меднения, теперь он готов к применению.
Хранение раствора и добавление формалина
В таком состоянии, то есть без формалина, раствор хранится очень долго, можно сразу размешать раствор на 5 литров, слить его в канистру и пользоваться им отливая нужное количество для меднения, добавляя в него формалин.
Для примера покажу как это делается.
Берем 20 мл. раствора химического меднения. По рецепту смотрим, что на 1 литр раствора нужно добавить 20 мл. формалина, произведем небольшой расчет.
Посчитаем сколько нужно формалина на 1 мл. раствора химического меднения.
20/1000 = 0,02 мл.
Так как мы взяли 20 мл. раствора хим. меднения, то..
20*0,02 = 0,4 мл. (0,4 кубика в шприце) формалина нужно добавить.
После добавления формалина, накрываем емкость крышкой. Накрываем что бы не нюхать запах формалина, берегите свое здоровье (формалин является канцерогеном!)
Данная статья опубликована на сайте . Постоянная ссылка на эту статью находится по этому адресу
Читайте статьи на сайте первоисточнике, не поддерживайте воров.
Тестирование раствора химического меднения
Чтобы протестировать как работает раствор химического меднения, берем активированный активатором диэлектрик (как активировать отверстия в печатных платах, читайте в этой статье) и опускаем в емкость. Буквально на глазах текстолит начинает темнеть и покрываться химической медью.
Процесс химического меднения должен длиться от 15 до 30 минут, и это время зависит от результата и качества покрытия, за которым вы должны следить. В процессе меднения идет газовыделение, плату нужно постоянно покачивать и переворачивать для равномерного распределения раствора по поверхности.
Прошло 20 минут, результат работы раствора на лицо, весь диэлектрик, включая отверстия, покрылся тонким 1 мкм. слоем меди и он готов к дальнейшему этапу — гальванике, этот этап подробно описан в этой статье.
Не фольгированный текстолит был взят для примера, некоторые подумают, таким образом можно не покупать фольгированный текстолит, а наращивать медь на голый диэлектрик и делать таким образом платы. Сразу хочу «обломать» вас, что бы наращивать медь на диэлектрик, нужно хорошо подготавливать поверхность, что в домашних условиях реализовать очень трудно. Так что не мучайтесь и делайте платы обычным способом, то есть, активируйте фольгированный текстолит.
Емкость раствора по меди
В заключении еще хотел добавить, расход этого раствора химического меднения берем из расчета 50 мл. раствора на 1 дм.кв. печатной платы. То есть 50 мл. раствора хватит омеднить двухстороннюю плату размером 10*10 см.
Раствор после добавления формалина будет еще жить дней 5, затем испортится.
Советую, если делаете ответственные платы, то лучше размешать с формалином свежую порцию раствора химического меднения.
Состав растворов для химического меднения.
Для осуществления процесса химического меднения рекомендуется много разнообразных растворов. В целом состав раствора химического меднения обычно включает в себя:
- соль двухвалентной меди (сульфат меди);
- комплексообразователь;
- восстановитель;
- ускоряющие и стабилизирующие добавки;
- гидроксид натрия для регулирования рН.
Виды растворов меднения различают по тому, какой используется комплексообразователь: виннокислый (тартратный), трилонатный (этилендиаминтетрауксусный), лимоннокислый, глицериновый и т.д.
Наибольшее распространение получил виннокислый раствор химического меднения. Он содержит тартрат калия-натрия, который образует с ионами меди прочный комплексный анион [CuC4H4O6(OH)2]2-. Значительное распространение получили также трилонатные растворы, содержащие комплексообразователь трилон Б (ЭДТА). Остальные растворы применяются ограниченно.
Кроме формалина в качестве восстановителей в процессе химического меднения могут использоваться гипофосфит, гидразин, боргидрид, однако растворы меднения на их основе уступают растворам с формалином по выраженности автокаталитических свойств у осаждаемой меди, а также по стабильности, и, поэтому, не нашли практического применения.
Стабилизаторами в растворе могут выступать различные тиосоединения: тиосульфат натрия, тиомочевина, сульфид свинца, цистин, роданин, 2-меркаптобензотриазол, диэтилдитиокарбамат, а также цианистые соединения, роданиды, фенантролины и их производные, полисульфиды, соединения селена, ртути, некоторые окислители (в т.ч. кислород), высокомолекулярные вещества. На виннокислые растворы химического меднения стабилизирующее действие оказывают аммиак и углекислый натрий.
Физиологическая роль меди.
Как и большинство поливалентных металлов медь играет важную роль в метаболизме животных.
а. Процессы кроветворения.
Медь стимулирует созревание ретикулоцитов (молодых эритроцитов) превращая поступающее с пищей железо в органически связанную форму.
б. Гормоны гипофиза.
Медь стимулирует выработку гормонов гипофиза, тем самым нормализируя работу эндокринной системы организма.
в. Ферменты.
Медь входит в большинство окислительных ферментов, усиливающих энергию дыхания, влияющих на белковый и углеводный обмен. Одним из самых важных считается цитохромоксидаза — фермент катализирующий финальный этап тканевого дыхания, осуществляющий перенос электронов цитохрома на кислород. Этот металл является важнейшим компонентом белка церулоплазмин, который ускоряет окисление полиаминов в плазме крови человека. Так же медь это неотъемлемая часть ферментов управляющих процессами окисления и выработки таких белков как коллаген, который является основой соединительных тканей в организме: сухожилий, хрящей, дермы и эластин, который наряду с коллагеном образует объемную сеть волокон, придающих прочность соединительной ткани. Из эластина также строятся волокна соединительных тканей, образующих внутренний слой (каркас) сосудов. Поэтому медьсодержащие препараты часто используют при лечении переломов и разрывов связок.
г. Защита организма.
Воздействуя вместе с аскорбиновой кислотой медь мешает проникновению в организм воспалителей и микробов. Во время инфекционных заболеваний, а также при особых формах цирроза печени наблюдается резкое увеличение медьсодержащих соединений в сыворотке крови.
д. Психологическое состояние.
После продолжительных исследований организма человека ученые сделали вывод, что медь оказывает влияние не только на физиологическое, но и на психологическое состояние человека. У людей склонных к агрессии в волосах содержится гораздо больше этого металла, чем у спокойных, сдержанных.
Технология меднения
Различают 2 типа медных электролитов: кислые и щелочные. В кислых электролитах нельзя получить прочно сцепленные медные покрытия на стальных и цинковых изделиях, так как в этом случае железо и цинк в контакте с медью растворяются — нарушается сцепление с покрытием. Для устранения этой особенности — необходимо первый тонкий слой меди (2—3 мкм) нанести в щелочном электролите, а в дальнейшем наращивать покрытие в более экономичном кислом электролите до заданной толщины. Цинковые изделия сложной формы меднить лучше всего в щелочных (цианистых) электролитах. Кислые электролиты меднения Наиболее распространены электролиты двух видов — сернокислые и борфтористоводородные. Наибольшее применение нашли сернокислые электролиты, отличающиеся простотой состава, устойчивостью и высоким выходом по току (до 100%). Перед меднением стальных деталей в кислых электролитах их предварительно меднят в цианистых электролитах или осаждают тонкий подслой никеля. Недостатком этих электролитов является невозможность непосредственного покрытия стальных и цинковых деталей вследствие контактного выделения меди, имеющей плохое сцепление с основным металлом, а также их незначительная рассеивающая способность и более грубая структура осадков по сравнению с другими электролитами. Щелочные электролиты меднения К щелочным электролитам меднения относятся цианистые, пирофосфатные и другие электролиты. Цианистые медные электролиты обладают высокой рассеивающей способностью, мелкокристаллической структурой осадков, возможностью непосредственного меднения стольных деталей. К недостаткам относятся низкая плотность тока и неустойчивость состава вследствие карбонизации свободного цианида под действием двуокиси углерода воздуха. Кроме того, цианистые электролиты характеризуются пониженным выходом по току (не более 60-70%)